Биология в лицее
Сайт учителей биологии МБОУ Лицей № 2 г. Воронежа, РФ ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Site biology teachers lyceum № 2 Voronezh city, Russian Federation
|
Неорганические вещества клетки. Вода Все имеющиеся в клетке соединения можно разбить на две группы: органические и неорганические. Неорганические вещества — это химические вещества, которые не являются органическими, то есть они не содержат углерода (кроме карбидов, цианидов, карбонатов, оксидов углерода и некоторых других соединений, которые традиционно относят к неорганическим).
Среднее содержание воды в клетках составляет 80% от их общей массы. Однако, в зависимости от таксономической и тканевой принадлежности клеток, а также их возраста и состояния содержание воды может изменяться в широких пределах.
Вода — универсальная среда живой материи на клеточном уровне. В клетке вода находится в двух формах: связанная (5%) — формирует гидратные оболочки ионов и молекул, и свободная (95%) — участвует в транспорте веществ цитоплазмы. 165 лет назад Гумбольт и Гей-Люссак доказали, что 2 атома водорода и атом кислорода, соединяясь в молекулу, рождают воду. Воде была дана волшебная власть стать соком жизни на Земле. (Леонардо да Винчи) Уникальные свойства воды определяются структурой её молекулы В молекуле воды один атом кислорода ковалентно связан с двумя атомами водорода. Положительные заряды сосредоточены у атомов водорода в силу электроотрицательности кислорода. Молекула представляет собой диполь. Молекула воды испытывает сильное электростатическое притяжение, образуя водородные связи с другими молекулами.
В молекуле воды один атом кислорода ковалентно связан с двумя атомами водорода. Из-за большой разности электроотрицательностей атомов водорода и кислорода электроны всех атомов, составляющих молекулу воды, сильно смещены в сторону кислорода. Вследствие этого атом кислорода приобретает частичный отрицательный заряд. Поэтому молекула воды — диполь: та часть молекулы, где находится водород, заряжена положительно, а часть, где находится кислород, — отрицательно. Физические и химические свойства воды во многом обусловлены наличием водородных связей между молекулами воды — диполями. Свойства воды В жидкой воде наряду с обычными молекулами Н2О содержатся ассоциированные молекулы, т. е. соединенные в более сложные агрегаты (Н2О)x благодаря образованию водородных связей. С повышением температуры водородные связи разрываются, и полный разрыв наступает при переходе воды в пар.
Вода обладает теплоёмкостью, то есть способностью поглощать теплоту при минимальном изменении собственной температуры. Высокая теплоёмкость и теплопроводность воды обеспечивают регуляцию температуры организма, предохраняя клетку от резких колебаний температур. Вода обладает большой теплотой испарения. Испарение сопровождается охлаждением, что обусловливает участие воды в терморегуляции организма. Благодаря своей способности образовывать слабые химические связи с другими веществами вода — прекрасный растворитель гидрофильных веществ. В виде ионов происходит клеточный транспорт веществ. Все вещества по отношению к воде делятся на гидрофильные и гидрофобные. Гидрофильные вещества (греч. hydor — вода и philia — любовь) — вещества, хорошо растворимые в воде. Гидрофильностью (хорошей смачиваемостью водой) обладают вещества с ионными кристаллическими решетками (оксиды, гидроксиды, силикаты, сульфаты, фосфаты, глины и т. д.), вещества с полярными группами —ОН, —СООН, —NO2 и др.
Гидрофобностью (плохой смачиваемостью) обладает большинство органических веществ с углеводородными радикалами, металлы, полупроводники и т. д. Понятия гидрофильности и гидрофобности относятся не только к телам и веществам, у которых они являются свойством поверхности, но и к отдельным молекулам, их группам, атомам, ионам. Значение воды Вода обеспечивает осмотическое поступление веществ в клетку, поддерживает тургор, изменяет плотность тканей. Под действием некоторых ферментов-катализаторов она вступает в реакции гидролиза, то есть в реакции, при которых к свободным валентностям различных молекул присоединяются группы OH- или H+ воды. В результате образуются новые вещества с новыми свойствами. Содержание воды в организме зависит от его возраста и метаболической активности. Биологическая роль воды в организме
Влаголюбивые представители флоры ярко-зелёной окраски (осока, камыш, лапчатка гусиная, мать-и-мачеха, конский щавель, крапива, папоротник) предпочитают расти там, где грунтовые воды подходят близко к поверхности земли. Отыскать на местности водоносные жилы, чтобы не промахнуться с рытьём колодца, можно и с помощью других народных примет. К примеру, давно замечено, что вишни и яблони плохо растут там, где грунтовые воды подходят близко к поверхности земли. А вот ива, верба, ольха, берёза, напротив, чувствуют себя в таких местах чудесно. Рыжие муравьи воду недолюбливают. В местах, где они устраивают свои муравейники, рыть колодец — дело почти безнадёжное: до воды не докопаешься. О "живой" и "мёртвой" воде В народных сказках часто встречаются сюжеты о «живой» и «мертвой» воде. Современная наука пришла к выводу, что аналоги этих сказочных веществ на самом деле существуют. Это так называемые «легкая» и «тяжелая» вода.
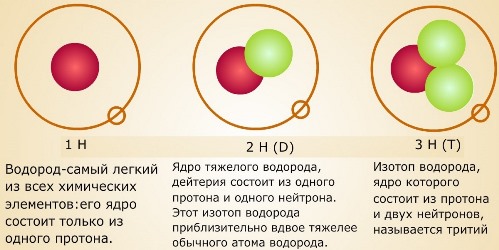
Таким образом, существуют три разновидности воды: обычная или лёгкая (1H216O); дейтериевая или тяжелая (D2O); тритиевая или сверхтяжелая (Т2О). Основную массу природной воды — свыше 99% — составляет лёгкая вода. Одна молекула тяжёлой воды приходится на 3200 молекул лёгкой, а сверхтяжёлой воды во всей гидросфере одновременно насчитывается лишь около 20 кг. Однако чистой 1H216O в естественных условиях не существует. Во всем мире такую воду получают в немногих специальных лабораториях, путем многократной очистки природной воды, или в результате синтеза.
Различается вода и по изотопному составу кислорода. Помимо кислорода 16O, в природе существуют еще два природных изотопа — 17O и 18O. В природных водах в среднем на каждые 10 тысяч атомов изотопа 16O приходится 4 атома изотопа 17O и 20 атомов изотопа 18O. По современным данным число изотопных разновидностей воды может достигать 135. Тяжелая вода применяется в ядерных реакторах для торможения нейтронов. А вот использование её для поливки растений приводило к прекращению их роста. Ещё более неутешительными были результаты опытов на животных: получая тяжёлую воду в больших концентрациях, животные погибали, когда половина воды в их теле была дейтерирована. Однако некоторые микроорганизмы хорошо себя чувствуют в 70% растворе D2O, а бактерии способны жить даже в чистой тяжёлой воде. «Легкая вода», где дейтерий и тяжелый кислород отсутствуют или их содержание значительно снижено, напротив, обладают целым рядом полезных биологических свойств. Экспериментально были получены результаты: мыши, получившие значительную дозу облучения, имели больший срок жизни, если они пили легкую воду. Кроме того, эксперименты показали, что «легкая вода» замедляет рост некоторых типов опухолей, стимулирует рост.
< Предыдущая страница "Химический состав клетки" Следующая страница "Неорганические вещества клетки. Минеральные соли" > |
Меню сайтаНаш опросМини-чатПоиск |
 Вода (оксид водорода, Н2O) — прозрачная жидкость, не имеющая цвета (в малом объёме) и запаха. В твёрдом состоянии называется льдом или снегом, а в газообразном — водяным паром. 71 % поверхности Земли покрыто водой (океаны, моря, озера, реки).
Вода (оксид водорода, Н2O) — прозрачная жидкость, не имеющая цвета (в малом объёме) и запаха. В твёрдом состоянии называется льдом или снегом, а в газообразном — водяным паром. 71 % поверхности Земли покрыто водой (океаны, моря, озера, реки).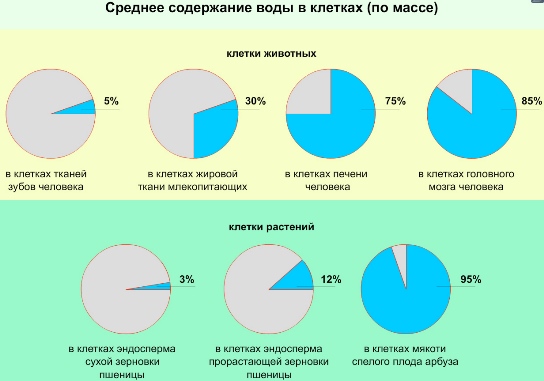
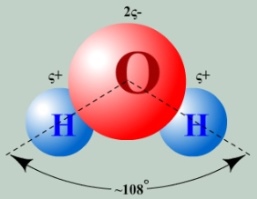 Молекула воды имеет угловую форму: атомы водорода по отношению к кислороду образуют угол, равный приблизительно 108°.
Молекула воды имеет угловую форму: атомы водорода по отношению к кислороду образуют угол, равный приблизительно 108°. 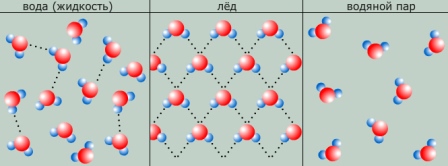
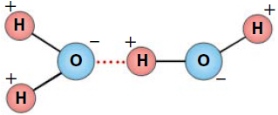 Наличием водородных связей между молекулами воды объясняются аномалии ее физических свойств:
Наличием водородных связей между молекулами воды объясняются аномалии ее физических свойств: Гидрофобные вещества (греч.
Гидрофобные вещества (греч.  Тридцатые годы ХХ века были ознаменованы огромным прорывом в физике элементарных частиц. В 1932 году русский физик Дмитрий Дмитриевич Иваненко и немецкий физик Вернер Гейзенберг независимо друг от друга предложили протонно-нейтронную модель ядра, согласно которой ядро состоит из положительно заряженных протонов и не имеющих заряда нейтронов. Число протонов в ядре соответствует числу нейтронов и равно зарядовому числу ядра. Согласно этой теории изотопы — это разновидности атомов (и ядер) одного химического элемента с разным количеством нейтронов в ядре. В этом же 1932 году американским учёным
Тридцатые годы ХХ века были ознаменованы огромным прорывом в физике элементарных частиц. В 1932 году русский физик Дмитрий Дмитриевич Иваненко и немецкий физик Вернер Гейзенберг независимо друг от друга предложили протонно-нейтронную модель ядра, согласно которой ядро состоит из положительно заряженных протонов и не имеющих заряда нейтронов. Число протонов в ядре соответствует числу нейтронов и равно зарядовому числу ядра. Согласно этой теории изотопы — это разновидности атомов (и ядер) одного химического элемента с разным количеством нейтронов в ядре. В этом же 1932 году американским учёным 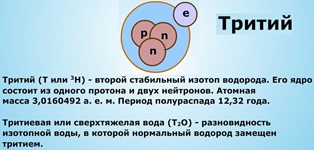 Занимаясь дальнейшими исследованиями, Юри обнаружил, что изотопы водорода могут входить в состав молекул воды вместе с обычными молекулами. Так была открыта «тяжёлая вода». А в 1933 году Гилберт Льюис получил чистую тяжёловодородную воду.
Занимаясь дальнейшими исследованиями, Юри обнаружил, что изотопы водорода могут входить в состав молекул воды вместе с обычными молекулами. Так была открыта «тяжёлая вода». А в 1933 году Гилберт Льюис получил чистую тяжёловодородную воду.